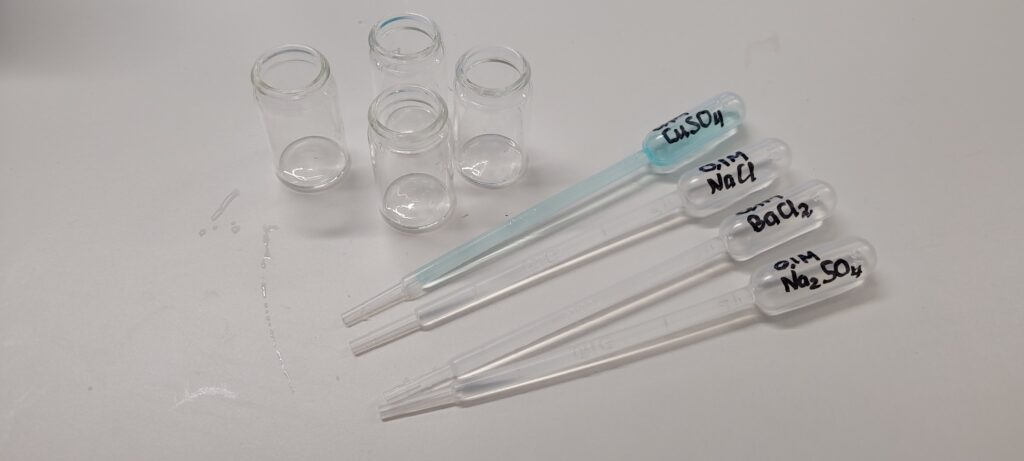
Dette trenger du
- 0,1 mol/L BaCl2 (ikke merkepliktig)
- 0,1 mol/L NaCl (ikke merkepliktig)
- 0,1 mol/L CuSO4 (giftig med langtidsvirkning for liv i vann)
- 0,1 mol/L Na2SO4 (ikke merkepliktig)
- Plastpipetter
- Vannfast tusj
- 6 små begerglass til å utføre reaksjonene i
Praktisk info: Rester etter fellingsreaksjonene tømmes i vasken. Eventuelle rester av 0,1 mol/L CuSO4 samles opp på resteflaske og og leveres som farlig avfall.
Forberedelse: Lage 0,1 mol/L BaCl2-løsning ved å løse 2,1 g av saltet i litt vann, og fortynne opp til 100 ml med vann.
Lage 0,1 mol/L NaCl-løsning ved å løse 5,8 g av saltet i litt vann, og fortynne til 100 ml med vann.
Lage 0,1 mol/L Na2SO4-løsning ved å løse 14,2 g av saltet i litt vann, og fortynne til 1 L med vann.
Lage 0,1 mol/L CuSO4-løsning ved å løse 2,5g CuSO4 5H2O(s) i litt vann og fortynne til 100 ml med vann. Det brukes her kobbersulfag med krystallvann. Det betyr at det er vannmolekyler inne i krystallstrukturen til saltet.
Litt av hver av de 4 salt-løsningene tilsettes til hver sin plastpipette, så skriver du den kjemiske formelen til saltet på plastpipetten med vannfast tusj.
Hensikt
I denne øvelsen skal elevene undersøke og sammenligne ulike salt-løsninger ved å gjøre systematiske observasjoner av kjemiske fellingsreaksjoner.
Ferdigheter
Ferdighetene som øves spesielt i denne øvelsen: observere, beskrive, systematisere, analysere data, oppdage, forklare
I denne øvelsen skal elevene øve på å gjøre systematiske observasjoner av kjemiske fellingsreaksjoner, og beskrive det de observerer med egne ord. Elevene vil oppdage nye fysiske og kjemiske egenskaper hos stoffene, og det vil kanskje dukke opp spørsmål som de ønsker svar på. I tillegg vil elevene øve på å forklare hva som skjer i en fellingsreaksjon ved å bruke ordlikninger og kjemiske formler. Elevene skal bruke kilder i form av en løselighetstabell. Sammenhengen mellom stoffers egenskaper på mikronivå og makronivå bør trekkes inn i diskusjonen med elevene. Det vitenskapelige produktet av denne utforskningen er data som angir ulike stoffers egenskaper, og eventuelt spørsmål og hypoteser som kan danne grunnlag for videre eksperimenter.
Slik gjør du
- Bruk brikkene: observere, beskrive, systematisere, analysere data, oppdage, forklare. Planlegg gjennomføringen sammen med elevene og snakk om hva de ulike ferdighetene innebærer. Er det en rekkefølge på de ferdighetene som øves? Hvordan henger de sammen tenker dere?
- I dette forsøket kan elevene gjerne jobbe sammen i par eller grupper. Del ut to små begerglass og fire plastpipetter som inneholder hver av de 4 salt-løsningene.
- Elevene skal skrive ned formlene til de 4 saltene i notatboka si. Det vil være lurt å skrive formlene under hverandre. Til høyre for formelen skal de skrive hvilke ioner som finnes i en vannløsning av hvert av de 4 saltene. Dette kan også gjøres felles på tavla i klassen.
- Be elevene observere og beskrive de fire ulike løsningene (saltet CuSO4 gir en blå løsning når det løses i vann).
- Elevene får beskjed om å velge to av saltløsningene som de ønsker å blande. La elevene blande litt av hver av de to saltløsningene i et lite begerglass, og be dem om å skrive ned sine observasjoner i boka si.
- Videre kan elevene blande to nye saltløsninger med hverandre, og fortsetter å skrive systematisk ned hvilke observasjoner de gjør.
- Når alle kombinasjonene av saltløsninger er blandet med hverandre, så kan elevene oppsummere sine observasjoner. Har det skjedd en fellingsreaksjon? Hvilke to salter blandet de for å få en utfelling?
- Elevene kan nå få delt ut løselighetstabellen som er vist under. De sammenlikner sine resultater med informasjonen i tabellen og skriver ned reaksjonslikningen for fellingsreaksjonen de har observert.
- Bruk de sekskantede brikkene og la elevene diskutere i grupper hvilke ferdigheter de har øvd på i denne øvelsen. Hvordan kan de bruke brikkene til å illustrere prosessen? På hvilke måter har de arbeidet med naturvitenskapelig praksiser og tenkemåter i denne øvelsen?
Faglig forklaring
Salter kalles også ioneforbindelser. Salter er forbindelser som består av ioner med motsatte ladninger, og ioner tiltrekkes av hverandre med elektrostatiske krefter. Et eksempel på et salt er saltet vi bruker i matlaging, nemlig natriumklorid med den kjemiske formelen NaCl. Dette saltet består av positivt ladede natriumioner (Na+), og negativt ladede kloridioner (Cl–). Det finnes mange millioner ulike typer salter. Noen salter er lettløselige i vann, andre er det vi kaller tungtløselige i vann, mens andre igjen er uløselige i vann. Disse kategoriene defineres slik:
Lettløselig salt: Det løses mer enn 1g av saltet i 100 ml vann.
Tungtløselig salt: Det løses mellom 0,01g og 1g av salter i 100 ml vann.
Uløselig salt: Det løses mindre enn 0,01g av saltet i 100 ml vann.
Hvilke salter som er lettløselige, tungtløselige og uløselige presenteres i form av en såkalt løselighetstabell (se under). Fra denne tabellen kan vi lese om et salt vil felles ut av løsningen som bunnfall når vi blander to lettløselige salter med hverandre.
| Cl– (fra NaCl eller BaCl2) | SO42- (fra Na2SO4 eller CuSO4) | |
| Na+ (fra NaCl eller Na2SO4) | Lettløselig | Lettløselig |
| Cu2+ (fra CuSO4) | Lettløselig | Lettløselig |
| Ba2+ (fra BaCl2) | Lettløselig | Uløselig |
Vi kan skrive løselighetsreaksjonene for de lettløselige saltene som inngår i denne øvelsen slik:
CuSO4(s) –> Cu2+(aq) + SO42-(aq)
NaCl(s) –> Na+(aq) + Cl–(aq)
BaCl2(s) –> Ba2+(aq) + 2Cl– (aq)
Na2SO4(s) –> 2Na+(aq) + SO42-(aq)
Reaksjonslikningen for fellingsreaksjonen:
Ba2+(aq) + SO42-(aq) –> BaSO4(s) Utfelling
Forslag til utvidelse
For å øke kompleksiteten på forsøket kan du benytte flere enn 4 beholdere med salt-løsninger. Det vil kreve at eleven gjør systematiske notater, og tolkning av en mere omfattende løselighetstabell for å finne ut om svaret en har fått stemmer med tabellverdiene.
Når elevene har fått øvelse med å skrive ned løselighetsreaksjoner og gjennomføre fellingsreaksjoner med kjente salter, så kan du f.eks. gjøre øvelsen om til en detektivoppgave ved at elevene ikke vet hvilken pipette som inneholder hvert av de 4 saltene. Elevene bør likevel kjenne til hvilke 4 salter som inngår i forsøket.
Hvis elevene har forhåndskunnskaper om syre-base-reaksjoner fra tidligere så kan du som lærer legge inn at elevene både må teste om stoffene i plastpipettene har syre-base-egenskaper, og at de må se etter tegn på utfelling for å finne identiteten til stoffene i de ulike beholderne.
Kilder
Inspirasjon til forsøket er hentet fra læreboka Kjemi for lærere av Merethe Hannisdal og Vivi Ringnes.